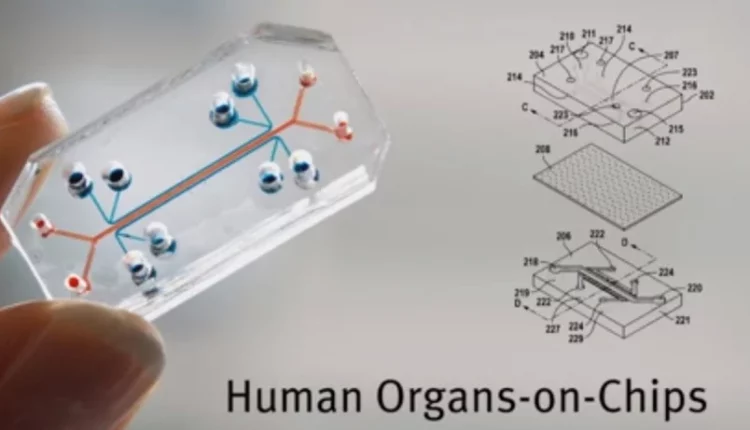
Η τεχνολογία «άνθρωπος σε τσιπ» μειώνει τις δοκιμές στα ζώα και σηματοδοτεί το μέλλον της έρευνας
Μικροτσίπ διασυνδεδεμένων ανθρώπινων κυττάρων, ιστών και οργάνων αντικαθιστούν τα ζωικά μοντέλα σε προκλινικές δοκιμές για την ανακάλυψη φαρμάκων και για τον έλεγχο της τοξικότητας ουσιών.
Πόσα ανθρώπινα όργανα χωρούν μέσα στο χέρι μας; Ακούγεται ως μια τρομακτική ερώτηση που (ελπίζουμε) πως δεν έχουμε σκεφτεί ποτέ. Ωστόσο αρκετοί επιστήμονες, όχι μόνο την έχουν σκεφτεί, αλλά έχουν αφιερώσει την περισσότερη έρευνά τους στη δημιουργία μιας τεχνολογίας που επιτρέπει σε ένα σύστημα ανθρώπινων οργάνων να αναδημιουργούνται σε μικρογραφία πάνω σε μικρο-ψηφίδες (μικροτσιπ), να διασυνδέονται μεταξύ τους και να χωρούν όλα μέσα στην παλάμη του ενός χεριού μας.
Οι ειδικοί μιλούν για ένα αναδυόμενο κίνημα βιοτεχνολογίας που υπόσχεται να μεταμορφώσει την ιατρική επιστήμη και να αναθεωρήσει ριζικά την επίπονη διαδικασία διάθεσης νέων φαρμάκων, τροφίμων και καλλυντικών στην αγορά.
Οι μικρο-ψηφίδες (μικροτσιπ) που διαθέτουν κανάλια/ θαλάμους της τάξης 1 μικρομέτρου μέχρι μερικών χιλιοστών για μεταφορά υγρών/ διαλυμάτων, προσφέρουν τη δυνατότητα μικροσκοπικής αναδημιουργίας ανθρώπινων οργανοειδών (μίνι οργάνων μεγέθους 1-3 χιλιοστών συνήθως). Μικροσκοπικές εκδοχές ήπατος, πνευμόνων, νεφρών και άλλων ζωτικών οργάνων κατασκευάζονται κατά τέτοιο τρόπο ώστε να αναπαράγουν ορισμένες από τις βασικές λειτουργίες των ανθρώπινων ομολόγων τους, όπως για παράδειγμα, τις αναπνευστικές κινήσεις ή τις μυϊκές συσπάσεις κυττάρων. Οι μικρο-ψηφίδες μπορούν επίσης να διασυνδέουν δύο, τρία ή και τέσσερα οργανοειδή και, μετά τη διοχέτευση σε αυτές φαρμάκων δοκιμαστικά, να επιτρέπουν στους επιστήμονες να παρατηρούν τον τρόπο που οι ουσίες αλληλεπιδρούν με αυτά τα μιμητικά ανθρώπινα όργανα.
«Με επιστημονικούς όρους, η τεχνολογία Human-on-a-chip (HoaC) μοντελοποιεί ανθρώπινα κύτταρα, ιστούς και οργανοειδή σε διασυνδεδεμένες in vitro μικρορευστονικές συσκευές, και έχει τη δυνατότητα να μειώσει το κόστος των προκλινικών μελετών και να αυξήσει το ποσοστό έγκρισης φαρμάκων εισάγοντας ανθρώπινα φαινοτυπικά μοντέλα στην έρευνα για σπάνιες ασθένειες και στην ανάπτυξη ορφανών φαρμάκων(που χρησιμοποιούνται για τη θεραπεία σπάνιων νόσων). Από την άλλη πλευρά, γίνεται πραγματικότητα η εξατομικευμένη ιατρική, δηλαδή η δυνατότητα του κάθε ατόμου-ασθενούς να λαμβάνει ξεχωριστή αγωγή (θεραπεία) που ταιριάζει αποκλειστικά στην περίπτωση και στις θεραπευτικές ανάγκες του», περιγράφει ο ερευνητής στο Ινστιτούτο Ηλεκτρονικής Δομής και Λέιζερ του Ιδρύματος Τεχνολογίας και Έρευνας (ΙΤΕ) και συνιδρυτής της ελληνικής ιατροτεχνολογικής εταιρείας BIOPIX-T, Δρ. Αλέξανδρος Πανταζής.

Αυτή η τεχνολογία θα μπορούσε να είναι η απάντηση σε μια συνεχιζόμενη κρίση στο πεδίο των δοκιμών φαρμάκων και χημικών ουσιών, όπου παρατηρείται έλλειψη ζωικών μοντέλων, των οποίων συχνά η προγνωστική αξία είναι χαμηλή, οδηγώντας σε μεταφραστική αποτυχία στον άνθρωπο. Τα ζωικά μοντέλα δεν μιμούνται με ακρίβεια τις ανθρώπινες φυσιολογικές αποκρίσεις ή δεν προβλέπουν με ακρίβεια την αποτελεσματικότητα και την τοξικότητα ενός φαρμάκου στον άνθρωπο λόγω των εγγενών βιολογικών διαφορών που υπάρχουν μεταξύ των ειδών σε γενετικό και ανατομικό επίπεδο, συμπεριλαμβανομένων της φαρμακοκινητικής, της φαρμακοδυναμικής (PK/PD), αλλά και της διάρκειας ζωής. Η ανάπτυξη φαρμάκων για σπάνιες νόσους παρεμποδίζεται και από άλλα ζητήματα που επηρεάζουν τη φαρμακευτική βιομηχανία, όπως το υψηλό κόστος διάθεσης νέων θεραπευτικών παραγόντων στην αγορά σε συνδυασμό με το χαμηλό ποσοστό επιτυχίας έγκρισης από τις ρυθμιστικές αρχές, κυρίως λόγω του περιορισμένου δείγματος ασθενών για τη διενέργεια στατιστικά σημαντικών κλινικών μελετών.
Σύμφωνα με την Ένωση Βιοϊατρικής Έρευνας της Καλιφόρνιας, χρειάζονται κατά μέσο όρο 12 χρόνια για να «ταξιδέψει» ένα φάρμακο από την προκλινική έρευνα στους ασθενείς, με μέσο κόστος 359 $ εκατομμύρια. Αν κάνει κάποιος τους υπολογισμούς για το 90% των φαρμάκων που δεν τα καταφέρνουν θα αντιληφθεί την ανάγκη για μια επαναστατική νέα προσέγγιση.
Υποκατάστατα ανθρώπινων οργάνων
Τις τελευταίες δεκαετίες, οι εξελίξεις στη νανοτεχνολογία, τη μικροκατασκευή και τις τεχνικές κυτταρικής βιολογίας επέτρεψαν την ανάπτυξη μικροφυσιολογικών συστημάτων (MPS), που ονομάζονται μοντέλα Organ-on-a chip (OOC) ή Body-on-a-chip (BoaC) όταν περιλαμβάνονται πολλά όργανα στην ίδια πλατφόρμα ή τελευταία Human-on-a-chip (HoaC).
Αυτές οι πλατφόρμες, όταν συνδυάζονται με την τεχνολογία επαγόμενων πολυδύναμων βλαστοκυττάρων (iPSC), παρέχουν την ευκαιρία καλλιέργειας κυττάρων ειδικά για κάθε ασθενή που διαφορετικά θα ήταν δύσκολο να αποκτηθούν στις μεγάλες ποσότητες που απαιτούνται για ερευνητικούς σκοπούς. Το πιο σημαντικό όμως είναι ότι επιτρέπεται η δημιουργία εξειδικευμένων κυττάρων χωρίς τις τεχνικές ή βιοηθικές ανησυχίες που πλαισιώνουν την απευθείας λήψη ανθρώπινων βλαστοκυττάρων.
Ο συνδυασμός της τεχνολογίας iPSC και της επεξεργασίας γονιδιώματος CRISPR/Cas9 («μοριακό ψαλίδι») έχει καταστήσει διαθέσιμες μοναδικές επιλογές κυττάρων, όπου μπορούν να προκληθούν ή να διορθωθούν γενετικές μεταλλαγές για τη μοντελοποίηση ασθενειών in vitro. Ο συνδυασμός έχει χρησιμοποιηθεί για τη δημιουργία γραμμών πολυδύναμων βλαστοκυττάρων (iPSC) που φέρουν μεταλλαγές για σπάνιες ασθένειες όπως η κυστική ίνωση, η νόσος Tay-Sachs, η οικογενής δυσαυτονομία, η μυϊκή δυστροφία και το σύνδρομο Barth.
«Η τεχνολογία HoaC συνδυάζει την κυτταρική καλλιέργεια με τα BioMEMs (βιοϊατρικά ή βιολογικά μικροηλεκτρομηχανικά συστήματα που επικεντρώνονται συνήθως περισσότερο σε μηχανικά μέρη, με τεχνολογίες μικροκατασκευής για να γίνουν κατάλληλα για βιολογικές εφαρμογές και με τη χημεία επιφανειών, επιτρέποντας τη φαινοτυπική μοντελοποίηση της στοιχειώδους φυσιολογίας οργάνων σε μια μικρορευστονική συσκευή», εξηγεί ο Δρ. Πανταζής και συνεχίζει: «Ο όρος μικρορευστονική (microfluidics) περιγράφει, τόσο την επιστήμη που μελετά τη συμπεριφορά των ρευστών, όταν αυτά περιορίζονται σε μικρές γεωμετρίες (με διαστάσεις της τάξης μερικών ή εκατοντάδων μικρόμετρων), όσο και την τεχνολογία κατασκευής μικροδιατάξεων, οι οποίες επιτρέπουν το χειρισμό και τον ακριβή έλεγχο μικρών όγκων ρευστών (της τάξεως των μικρολίτρων)»
Μοντέλα tailor made
Τα μοντέλα Human-on-a chip (HoaC ) πολλαπλών οργάνων ενσωματώνουν δύο ή περισσότερους ιστούς ή τύπους κυττάρων για να μοντελοποιήσουν τη σχέση μεταξύ των οργάνων. Αυτά τα συστήματα μιμούνται τις in vivo επιδράσεις των ειδικών για τα όργανα κυτοκινών στο σώμα ή των μεταβολιτών του φαρμάκου που παράγονται από το ήπαρ σε άλλα όργανα.
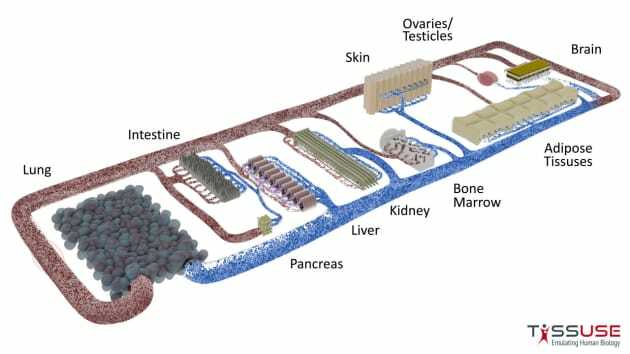
Ενδεικτικά, για αυτόν το σκοπό, το εργαστήριο Καθηγητή Βιοιατρικής Μηχανικής Mike Shuler στο Πανεπιστήμιο Cornell έχει προτείνει ένα μοντέλο HoaC δεκατριών οργανοειδών που διατηρεί τη βιωσιμότητα όλων των τύπων κυττάρων έως και 7 ημέρες. Επίσης, μια άλλη εταιρεία, η CN Bio, που είναι κορυφαία εταιρεία ανάπτυξης μικροφυσιολογικών συστημάτων μονού και πολλαπλών οργανοειδών (MPS) έχει επιδείξει το πιο ολοκληρωμένο Human-on-a Chip με την ονομασία PhysioMimix OOC Multi-Organ MPS, το οποίο περιλαμβάνει δέκα συστήματα διασυνδεδεμένων οργανοειδών.
Μικρορευστονικά συστήματα ως μοντέλα ενός μεμονωμένου ή πολλαπλών οργανοειδών, έχουν ήδη αναπτυχθεί για τον λευκό λιπώδη ιστό, για την καρδιά, το ήπαρ, τους σκελετικούς μύες, τον πνεύμονα, τον γαστρεντερικό σωλήνα, τα νεφρά τα αναπαραγωγικά όργανα, το κεντρικό και το περιφερικό νευρικό σύστημα, το δέρμα και τα οστά.
Έχουν επίσης αναπτυχθεί μοντέλα HoaC που μιμούνται τη φυσιολογία του ιστού φυσιολογικών φραγμών ουσιών, όπως για παράδειγμα της γαστρεντερικής οδού, του πνευμονικού επιθηλίου και του αιματοεγκεφαλικού φραγμού, επιτρέποντας τη μοντελοποίηση συγκεκριμένων βιολογικών διεργασιών, όπως η εισβολή όγκου και η διείσδυση ουσιών στο δέρμα.
Ένα τέτοιο μοντέλο ανθρώπινου εγκέφαλου σε τσιπ (Brain-Chip) που βασίζεται στην τεχνολογία Organs-on-Chip παρουσίασε πέρσι η spinoff εταιρεία Βιοτεχνολογίας Emulate του Πανεπιστημίου Harvard. «Αναπτύξαμε μικροτσιπ, μεγέθους ενός στικ μνήμης ηλεκτρονικού υπολογιστή, τα οποία περιέχουν μικροσκοπικά κανάλια που είναι επενδυμένα με ανθρώπινα κύτταρα και τεχνητό ιστό αιμοφόρων αγγείων. Το Brain-Chip σχεδιάστηκε για να προσομοιώσει την πολυπλοκότητα του ανθρωπίνου αιματοεγκεφαλικού φραγμού και περιλαμβάνει νευρώνες, αστροκύτταρα, μικρογλοία, περικύτταρα, και μικροαγγειακά ενδοθηλιακά κύτταρα από τον άνθρωπο (Human iPSCs), επιτρέποντας τη διερεύνηση της ασφάλειας και της αποτελεσματικότητας θεραπειών in vitro, στο εργαστήριο», εξηγεί ο Δρ. Ιωσήφ Πεδιαδιτάκης συστήνοντας τη νέα καινοτομία που αναδείχθηκε ως μία από τις δέκα σημαντικότερες για το 2021 από το περιοδικό The Scientist, προσφέροντας ελπίδα σε ασθενείς με σοβαρές νευρολογικές διαταραχές, όπως τη νόσο του κινητικού νευρώνα (ALS), το Αλτσχάιμερ και την Πάρκινσον.

Η έρευνα, στην οποία συμμετείχαν πολλοί Έλληνες Καθηγητές και ερευνητές δημοσιεύτηκε στο έγκριτο περιοδικό Nature Communications, (https://www.nature.com/articles/s41467-021-26066-5). Ο Δρ. Πεδιαδιτάκης κατέχει σήμερα τη θέση του Associate Director της εταιρείας Vesalius Therapeutics Inc., που ιδρύθηκε από την venture capital Flag ship Pioneering. Από το έτος 2017 μέχρι το 2021 διατέλεσε Associate Director της εταιρείας Emulate, Inc. (Βοστώνη, Η.Π.Α) και ηγήθηκε της ανάπτυξης του Brain-Chip.
Πρωτοπόρες εταιρείες
Το 2012, η τεχνική πρόοδος στο πεδίο των μικροφυσιολογικών συστημάτων άνοιξε δρόμο στις πρωτοβουλίες «Microphysiological Systems for Drug Efficiency and Toxicity Testing Program» από τα NIH (Εθνικά Ινστιτούτα Υγείας) και την DARPA (Υπηρεσία Έρευνας Προηγµένων Αµυντικών Προγραµµάτων) των ΗΠΑ και ενθάρρυνε την ωρίμανση και την εμπορευματοποίηση αυτής της τεχνολογίας.
Η Hesperos Inc. ήταν η πρώτη spin-off εταιρεία που προέκυψε από την πρωτοβουλία NIH/DARPA και η πρώτη που το 2018 έφτασε την τεχνολογία της στη φάση IIb της χρηματοδότησης από το Εθνικό Κέντρο για την Προώθηση Μεταφραστικών Επιστημών (National Center for Advancing Translational Sciences (NCATS), το οποίο δύσκολα χρηματοδοτεί νεοφυείς εταιρείες βιοτεχνολογίας.
Η πρωτοπόρα Hesperos Inc. που δημιούργησαν ο καθηγητής Νανοτεχνολογίας James “J” Hickman και ο καθηγητής Βιοιατρικής Μηχανικής Mike Shuler αναπτύσσει εμπορικά σχεδόν τη τελευταία δεκαετία τις πρωτοποριακές συσκευές τις στις εγκαταστάσεις της στο Ορλάντο, στη Φλόριντα. Η εταιρεία προσφέρει τέσσερα βασικά επικυρωμένα συστήματα Human-on-a-Chip για μοντελοποίηση ασθενειών και δοκιμές φαρμάκων: Μοντέλο δύο οργάνων καρδιάς-ήπατος (Heart-Liver,Two Organ Model), Μοντέλο δύο οργάνων Νευρομυικής σύνδεσης (Neuromuscular Junction (NMJ) Two-Organ Model), Μοντέλο τεσσάρων οργάνων καρδιάς-ήπατος-σκελετικού μυός-νευρώνα (Heart-Liver-Skeletal Muscle-Neuron Four Organ Model) και Μοντέλο τριών οργάνων καρδιάς-ήπατος-καρκίνου (Heart-Liver-Cancer Three Organ Model).
Οι συνεργασίες με την AstraZeneca, τη Roche και με άλλες φαρμακευτικές οδήγησαν σε έρευνα για διάφορες θεραπείες, από αυτοάνοσες ασθένειες, στη νόσο του Αλτσχάιμερ και έως τον καρκίνο. Το 2021, τα δεδομένα αποτελεσματικότητας του μικροφυσιολογικού συστήματος της εταιρείας οδήγησαν στην έγκριση μιας κλινικής μελέτης (NCT04658472) μέσω της συνεργασίας με τη Sanofi . Το προτεινόμενο μικροφυσιολογικό σύστημα αφορά τα νευροφυσιολογικά χαρακτηριστικά δύο σπάνιων αυτοάνοσων απομυελινωτικών νευροπαθειών και καταδεικνύει την πιθανή χρήση του για την αξιολόγηση νέων θεραπευτικών μεθόδων. Η έρευνα δημοσιεύτηκε στο Advanced Therapeutics. https://doi.org/10.1002/adtp.202200030
Αντίστοιχα, η Cantex Pharmaceuticals, Inc., μια φαρμακευτική εταιρεία με έδρα στο Weston, FL μαζί με το Wyss Institute for Biologically Inspired Engineering στο Πανεπιστήμιο του Χάρβαρντ ανακοίνωσαν πρόσφατα ότι εξασφάλισαν παγκόσμια άδεια από το Γραφείο Ανάπτυξης Τεχνολογίας του Πανεπιστημίου του Χάρβαρντ (OTD) για να ξεκινήσουν κλινικές μελέτες φάσης ΙΙ για την ουσία azeliragon, που προορίζεται για φλεγμονώδεις πνευμονικές νόσους συμπεριλαμβανομένης της COVID-19. Μελέτες σε Organ-on-a Chip έδειξαν ότι η ουσία μπορεί να μειώσει δραματικά τις φλεγμονές ιικής προέλευσης στον ανθρώπινο πνευμονικό ιστό.


